水素の性質と活用
元素としての水素 [1]
物質としての水素 [2]
地球上にある水素の大部分は、化合物として存在しています。
水が「H2O」という分子記号で示されることはよく知られています。これは、水素原子2個と酸素原子1個が結合して、水という分子ができていることを意味しています。また天然ガスの主成分であるメタンはCH4という記号であらわされますが、これは炭素原子1個、水素原子4個からできています。このように水素は化合物として存在しています。水素は一つの原子では不安定なため、単独の場合には2原子が結合した水素分子(H2)として安定に存在することから、一般的に水素と呼んでいるのはこの水素分子です。自然界にはほとんど存在しておらず、他の化合物から人工的に作り出されて利用さています。
水素の形態として地球上で一番多いのは水です。ちなみに「水素」という名前は、水を構成する元であるということがその由来で、英語のhydrogenも、水(hydro)の元(gen)という意味です。
さまざまな用途に活用される水素
水素は産業用途として、肥料製造や半導体加工、さらに石油化学工業などで広く使われていますし、日常で広く使用されているニッケル水素電池という二次電池にも使われています(表)。すでに広く普及している家庭用燃料電池(エネファーム)では、都市ガスやLPGを原料に水素を製造し、その水素と空気で発電を行っています。
なお水素は、日本でも初期のガス灯や都市ガスに広く利用されていました(水素と一酸化炭素の混合ガスで、石炭から製造されていました)。一酸化炭素中毒の問題もあり、液化天然ガスの輸入開始とともに天然ガスに置き換わっていきましたが、それまで水素は身近な存在でした。
表 水素の主な利用方法
| 化学製品原料 | アンモニア肥料、合成樹脂、メタノール、医薬品、過酸化水素 |
|---|---|
| 化学加工用 | 脱硫、漂白殺菌、油脂硬化、半導体加工 |
| 熱利用 | 石英ガラス溶融、合金の焼結、溶接、照明(ライムライト) |
| 化学分析用 | ガスクロマトグラフィー分析 |
| 浮力利用 | 観測用気球、飛行船 |
| 燃料用 | 液体ロケット燃料 |
| 電力 | ニッケル水素電池、燃料電池 |
より詳しく知りたい
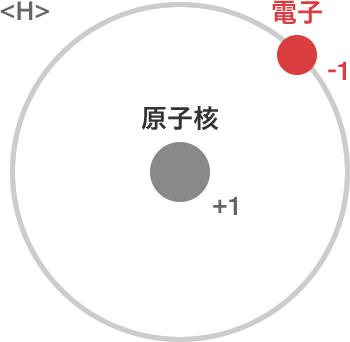
水素原子をモデル化した図。原子の中心にある原子核は陽子が一つだけで、電子がその周りに一個存在している。

工業用に販売されている、水素ボンベ。窒素や酸素など、ほかの物質と区別するためボンベは赤色に塗装されている。[4]
原子の大きさ(半径)は約1億分の1cmと非常に小さいのですが、その中はさらに原子核と電子に分かれ、さらに原子核は陽子と中性子で構成されています。このうち、陽子は+の電荷を、電子は-の電荷をそれぞれ持っています。
陽子や中性子と比べ電子の大きさははるかに小さく、太陽の周りを地球が回るように、原子内では原子核の周りを電子が回るような形で存在しています。
原子は、原子内の陽子数で化学的性質が決まりますので、陽子数で番号が付けられており、原子番号と呼ばれています。
水素は、さまざまな元素のなかでも陽子が1個だけ含まれる一番シンプルな原子構造で、原子番号は1です。
ごく一部の元素(ヘリウム等の不活性元素)を除き、原子は1つずつバラバラな状態ではとても不安定です。そこで、ほとんどの原子はいくつかの原子同士がくっついた分子、または沢山の原子が規則的に並ぶ結晶や金属と呼ばれる状態になります。水素の場合、原子2個のペアで安定な水素分子を形成し、これが一般的に水素と呼ばれています。そのほか、水素2個と酸素1個が結合した水分子、水素4個と炭素1個が結合したメタン分子などになります。さらにタンパク質や脂肪など私たちの体を作っている物質は、水素と炭素に加え窒素や硫黄などが複雑に組み合わさった分子からできていて、そこでも水素は重要な役割を果たしています。
水素分子は通常の状態(常温・常圧)では気体で、無色透明で臭いもありません。水素の一番大きな特徴は軽いことで、1ℓの重量はわずか0.089gと大気の15分の1程度の重量しかありません。また、その軽さが主な原因で、温度を下げてもなかなか液体や固体へと変化することがありません。1気圧の状態で水素を液化するためには-253℃といった低温まで冷やす必要があります。[7] 一般的には水素は、気体の状態で高圧ボンベに詰め込んだ状態で利用されています。[8]
純物質が天然に存在しなかったため、水素が発見されたのはかなり遅く、18世紀末になってのことでした。この際、水酸化ナトリウムという強アルカリ性物質を水に溶かし、直流電流を流すことで水を水素と酸素に分解しました。[9] この方法は、現在でも水電解法と呼ばれ、水素を作る主な技術として活用されています。
また天然ガスや石炭、石油などの有機物質を化学的に分解して水素を取り出すことも可能で、工業的にはこの方法で大量に作られています。[10]
文献リスト
- [1] 井口洋夫(1978)『元素と周期律』裳華房
- [2] コットン・ウィルキンソン(1987)『無機化学』培風館
- [3] 日本学術振興会「水の先進理工学」に関する先導的研究開発委員会(2011)
『基礎からわかる水の応用工学』p.3, 日刊工業新聞社 - [4] 容器保安規則(昭和41年5月25日通商産業省令第50号)第10条
- [5] 江沢洋(2013)『だれが原子をみたか』岩波書店
- [6] 国立天文台(2013)『理科年表 平成26年』p.383-丸善
[7][6]p.407 - [8] 岩谷産業(2014)『水素エネルギーハンドブック』p.12, http://www.iwatani.co.jp/jpn/h2/pdf/hydrogen_handbook.pdf
- [9]ウィークス・レスター(1988)『元素発展の歴史 1』pp.193-200, 朝倉書店
[10][8]p.10
